domingo, 30 de junio de 2013
BIENVENIDA
BIENVENIDA
bienvenidos a mi nuevo blog con temas de los cueerpos y la materia podran encontrar todo tipo de informacion de acuerdo al tema
ADELANTE!
ESTADOS FISICOS DE LA MATERIA
SUSTANCIAS PURAS Y MEZCLAS
PROPIEDADES DE LA MATERIA
LEY PERIODICA
Ley periodica
La ley periódica es la base de la tabla periódica de los elementos. Esta ley señala que las propiedades químicas y físicas de los elementos tienden a repetirse de manera sistemática a medida que se incrementa el número atómico. La tabla, por lo tanto, es una especie de esquema que se encarga de ordenar los elementos químicos de acuerdo al orden creciente de los números atómicos.
Un químico británico llamado John Alexander Reina Newlands (1838-1898) fue uno de los precursores de este concepto al proponer la ley de las octavas, que indicaba que cada ocho elementos se encuentran propiedades similares. Bajo esta idea, Newlands elaboró una tabla periódica en 1863.
El químico alemán Julius Lothar Meyer (1830-1895) se basó en estas nociones para descubrir los volúmenes atómicos de los elementos. Tras calcular los diferentes pesos atómicos y realizar gráficos con dichos valores, este experto logró demostrar que el aumento del peso atómico se correspondía a un incremento de las propiedades físicas. Los trabajos de Meyer respecto a la ley periódica fueron publicados en 1870.
El químico ruso Dmitri Mendeleiev (1834-1907), sin embargo, es quien se ha quedado con el mérito histórico como creador de la tabla periódica de los elementos. Su trabajo consistió en ordenar los elementos de acuerdo a su masa atómica y situar en una misma columna aquellos que tenían algo en común. Su tabla, presentada en 1869, se basó en la alteración manual de las propiedades químicas.
Las columnas verticales de la tabla periódica se conocen como grupos e incluyen elementos con idéntica valencia atómica (y que, por lo tanto, presentan propiedades parecidas entre sí). Las filas horizontales, por su parte, reciben el nombre de periodos y agrupan los elementos con propiedades que son diferentes pero cuyas masas resultan similares.
La Ley de Moseley
Esta ley empírica, cuya autoría pertenece al físico de origen británico Henry Moseley en el año 1913, define que cuando un átomo emite un rayo X existe una relación de tipo sistemática entre su número atómico y la longitud de onda.
La importancia de dicha ley reside en que dejó atrás la noción de que el número atómico fuera simplemente la representación del puesto que tenía cada elemento en la tabla periódica, el cual había sido asignado casi sin motivo específico por Mendeleiev.
A partir de entonces, Moseley emprendió un número de experimentos para confirmar el modelo del átomo de Bohr (propuesto también en 1913 por el físico danés de nombre Niels y que plantea que los electrones pueden orbitar de manera estable alrededor del núcleo atómico, entre otras cosas de gran importancia) en energías de rayos X, partiendo de la medición de las frecuencias que se originan en las transiciones electrónicas que sufren los átomos pesados.
La mesa en forma de tabla periódica
Mientras que la tabla periódica representa una pesadilla para muchos estudiantes de secundario, genera en otras personas una fascinación más allá de lo imaginable. Es el caso de Theodore Gray, cofundador de Wolfram Research, una de las más respetadas compañías de software e innovación científica y técnica, quien en el año 2002 construyó una mesa con forma de tabla periódica, que contiene muestras de cada elemento ubicadas de acuerdo a la distribución de Dmitri Mendeleiev.
Su trabajo no terminó allí, sino que comenzó a distribuir distintos diseños de su creación a museos y escuelas, haciendo especial hincapié en la importancia de apreciar los elementos en vivo y en directo, al contrario de simplemente ver su nomenclatura en un papel. Aunque este hombre no cuente con la fama de un cantante popular, su activa colaboración con la ciencia es muy reconocida entre las personas que gustan de esta rama del conocimiento, y en Internet existe muchísima información acerca de él y sus descubrimientos.
propiedades de la materia
Materia es todo aquello que tiene localización espacial, posee una cierta cantidad de energía, y está sujeto a cambios en el tiempo y a interacciones con aparatos de medida. En física y filosofía, materia es el término para referirse a los constituyentes de la realidad material objetiva, entendiendo por objetiva que pueda ser percibida de la misma forma por diversos sujetos. Se considera que es lo que forma la parte sensible de los objetos perceptibles o detectables por medios físicos. Es decir es todo aquello que ocupa un sitio en el espacio, se puede tocar, se puede sentir, se puede medir, etc.
La materia másica está jerárquicamente organizada en varios niveles y subniveles. La materia másica puede ser estudiada desde los puntos de vista macroscópico y microscópico. Según el nivel de descripción adoptado debemos adoptar descripciones clásicas o descripciones cuánticas. Una parte de la materia másica, concretamente la que compone los astros subenfriados y las estrellas, está constituida por moléculas, átomos, e iones. Cuando las condiciones de temperatura lo permite la materia se encuentra condensada.
Nivel microscópico
El nivel microscópico de la materia másica puede entenderse como un agregado de moléculas. Éstas a su vez son agrupaciones de átomos que forman parte del nivel microscópico. A su vez existen niveles microscópicos que permiten descomponer los átomos en constituyentes aún más elementales, que sería el siguiente nivel son:
Electrones: partículas leptónicas con carga eléctrica negativa.
Protones: partículas bariónicas con carga eléctrica positiva.
Neutrones: partículas bariónicas sin carga eléctrica (pero con momento magnético).
A partir de aquí hay todo un conjunto de partículas subatómicas que acaban finalmente en los constituyentes últimos de la materia. Así por ejemplo virtualmente los bariones del núcleo (protones y neutrones) se mantienen unidos gracias a un campo escalar formado por piones (bosones de espín cero). E igualmente los protones y neutrones, sabemos que no son partículas elementales, sino que tienen constituyentes de menor nivel que llamamos quarks (que a su vez se mantienen unidos mediante el intercambio de gluones virtuales).
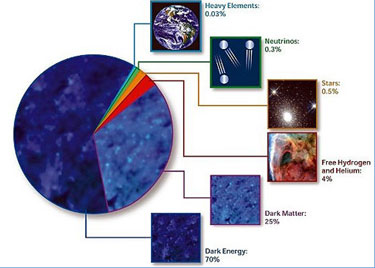
Distribución de materia en el universo
Según estimaciones recientes, resumidas en este gráfico de la NASA, alrededor del 70% del contenido energético del Universo consiste en energía oscura, cuya presencia se infiere en su efecto sobre la expansión del Universo pero sobre cuya naturaleza última no se sabe casi nada.
Según los modelos físicos actuales, sólo aproximadamente el 5% de nuestro universo está formado por materia másica ordinaria. Se supone que una parte importante de esta masa sería materia bariónica formada por bariones y electrones, que sólo supondrían alrededor de 1/1850 de la masa de la materia bariónica. El resto de nuestro universo se compondría de materia oscura (23%) y energía oscura (72%).
A pesar que la materia bariónica representa un porcentaje tan pequeño, la mitad de ella todavía no se ha encontrado. Todas las estrellas, galaxias y gas observable forman menos de la mitad de los bariones que debería haber. La hipótesis principal sobre el resto de materia bariónica no encontrada es que, como consecuencia del proceso de formación de estructuras posterior al big bang, está distribuida en filamentos gaseosos de baja densidad que forman una red por todo el universo y en cuyos nodos se encuentran los diversos cúmulos de galaxias. Recientemente (mayo de 2008) el telescopio XMM-Newton de la agencia espacial europea ha encontrado pruebas de la existencia de dicha red de filamentos.
Sustancias puras y m ezclas
1.
Clasificación de la materia
1.1.
La materia y sus propiedades
La materia es todo lo que nos rodea. Posee masa y ocupa un lugar en el espacio. La
materia puede describirse midiendo el
valor de sus propiedades; por ejemplo: la densidad,
el color, la masa, el volumen, etc.
Estas propiedades de la materia se clasifican en
propiedades generales
y
propiedades
características
. Las propiedades generales son comunes a todo tipo de materia y no
nos
sirven para identificarla (masa, volumen, longitud, temperatura) mientras que las
propiedades características tienen un valor propio para cada sustancia y nos sirven para
identificarlas (densidad, color, conductividad, temperatura de fusión).
La princi
pal división que se hace de la materia es en
sustancias puras
y
mezclas
de
sustancias puras. Las sustancias puras tienen unas propiedades características propias;
mientras que, las mezclas, no.
Por ejemplo, si tenemos un vaso con agua y otro que tiene agua
y sal podemos
distinguirlos basándonos en propiedades características.
Las propiedades características del agua son: densidad de 1 g/cc, temperatura de fusión
de 0 ºC y de ebullición de 100 ºC a la presión atmosférica. La mezcla de agua y sal tendrá
una d
ensidad, un punto de fusión y un punto de ebullición cuyos valores dependerán de la
proporción en que se encuentren sus componentes.
1.2.
Sustancias puras
Una sustancia pura es aquella cuya
composición no varía
, aunque cambien las
condiciones físicas en que se encuentre. Por ejemplo, el agua tiene una fórmula que es
H
2
O y es si
empre la misma, lo que indica que está formada por moléculas en las que hay 2
átomos de hidrógeno y 1 átomo de oxígeno. Si cambiara esa fórmula, sería otra sustancia
diferente.
Una sustancia pura
no se puede descomponer
en otras sustancias más simples
utilizando métodos físicos
.
Una sustancia pura tiene
propiedades características propias
o definidas.
Dentro de las sustancias puras se distinguen 2 tipos: Elementos y compuestos.
Los elementos son sustancias puras que
no se pueden descomponer en otras m
ás
simples por ningún procedimiento.
Están formadas por un único tipo de átomo. Son
todos los de la tabla periódica. En su fórmula química solo aparece el símbolo de un
elemento. Ej: octoazufre (S8), dihidrógeno (H2), dioxígeno (O2), hierro (Fe).
En la naturaleza, podemos encontrar 91 elementos diferentes y, de forma artificial, se han
obtenido casi treinta más, aunque son muy inestables. Todas las demás sustancias que
conocemos se forman por combinación de esos 91 elementos.
1.3.
Mezclas
Una mezcla es la combinación de
dos o más susta
ncias puras que se pueden separar
mediante métodos físicos
. No tiene propiedades características fijas, depende de su
composición. Su composición puede variar.
Podemos diferenciar dos tipos de mezclas: heterogéneas y homogéneas.
Una
mezcla heterogénea
es una mezcla en la que es posible distinguir sus componentes
a simple vista o mediante procedimientos ópticos. Ejemplo: Agua y aceite, granito, etc.
En esta mezcla heterogénea
formada por aceite y agua,
pueden distinguirse sus
componentes,
perfectamente, a
simple vista. Puede verse la
capa de agua en la parte
inferior (tiene mayor densidad)
y la capa de aceite en la parte
superior (tiene menor
densidad).
En este caso, ambos
componentes (aceite y agua),
son inmiscibles entre sí y por
ello se
observa que están
perfectamente separados.
Una
mezcla homogénea
es una mezcla en la que no es posible distinguir sus
componentes ni a simple vista ni a través de ningún procedimiento óptico. Este tipo de
mezcla también se llama
disolución
. Ejemplo: agua con azúcar, aire, acero, etc.
En estas mezclas homogéneas o
disoluciones se puede observar el
mismo aspecto en toda la mezcla.
No es posible distinguir sus
componentes a simple vista. La
única forma de diferenciar una
mezcla homogénea de una
sustancia pura es midiendo sus
propiedades características. En una
disoluc
ión, estas propiedades
varían en función de las
concentraciones de los
componentes
2.
Separación de
mezclas heterogéneas
Las sustancias puras que constituyen una mezcla pueden separarse mediante métodos
físicos. El método empleado depende del estado y propiedades de las sustancias que
queremos separar.
2.1.
Criba
La criba es un procedimiento que se emplea para
separar mezclas heterogéneas
sólidas
donde uno de los componentes tiene un tamaño muy distinto al otro. Ej: Arena y
piedras.
Empleado para separar sustancias
sólidas que tengan distinto tamaño,
como la
arena de la grava cuando se
desea preparar mortero en la
construcción. Como la grava está
formada por piedras de varios
centímetros de tamaño y la arena por
granos de apenas unos milímetros,
empleando una criba, que tiene una red
con agujeros de medio cent
ímetro, los
granos de arena atraviesan la criba
mientras que la grava no puede
atravesarla y, así, se separan.
Dependiendo del tamaño de los granos
a separar se puede emplear un tamaño
de agujero menor, en cuyo caso, el
instrumento que sirve para separar s
e
llama tamiz, en lugar de criba.
Estados Fisicos de la materia
Hay cinco estados principales de la materia: sólidos, líquidos, gases, plasmas y condensado de Bose-Einstein (BEC). Algunos de ellos son intermediarios o poco conocidos. En la actualidad se describen apenas tres estados en las versiones más populares: sólido, líquido y gas. Son todos diferentes estados de la materia.
Como se ha mencionado, se reconocen al menos tres estados de la materia: el estado sólido, el estado líquido y el estado gaseoso. En el caso de los vapores –que son un estado intermediario entre el estado líquido y el gaseoso –no existe capacidad para regresar directamente al estado líquido; ya cuando alcanza la forma de vapor puede ir al estado líquido a condición del intercambio de energía necesario para tal hecho; por ello se dice comúnmente vapor de agua.
El plasma es un estado en que la mayoría de la materia se encuentra en el Universo. En este estado hay una cierta ‘pastosidad’ de la sustancia, que permite una mayor y mejor respuesta cuando recibe informaciones decodificadas por los haces de luz emitidos a través de los componentes de la televisión. Se sabe que cualquier sustancia puede existir en tres estados: sólido, líquido y gaseoso, cuyo ejemplo clásico más inmediato es el agua en sus diversas formas (hielo, agua en estado líquido y vapor de agua). Todavía existen pocas sustancias halladas en esos estados, incluso tomando el Universo en su conjunto. Es poco probable que superen lo que en química se considera como restos infinitamente pequeños. Toda sustancia restante subsiste en el estado denominado plasma.
En el estado sólido se considera que el material del cuerpo macroscópico mantiene la forma y las posiciones relativas de sus partículas. Es particularmente estudiado en las áreas de la estática y la dinámica.
En el estado líquido, el cuerpo mantiene su cantidad de material a aproximadamente su volumen. La forma y la posición relativa de sus partículas son variables. Es particularmente estudiado en el campo de la hidrostática e hidrodinámica.
En el estado gaseoso, el cuerpo retiene sólo la cantidad de materia, pudiendo variar ampliamente en forma y volumen. Es particularmente estudiado en las áreas de aerostática y aerodinámica.
El Condensado de Bose-Einstein tiene características tanto de estado sólido y estado líquido, como de superconductividad y superfluidad, aunque, es encontrado en temperaturas extremadamente bajas (cercanas al cero absoluto) lo que hace que sus moléculas entre en colapso. Es particularmente estudiado en la mecánica cuántica.
Suscribirse a:
Comentarios (Atom)